3, 鉴别铬酸钡和铬酸铅的方法

流程分析可知,铬污泥(主要成分为Cr2O3,杂质为Fe2O3、Al2O3、SiO2)为原料粉碎后在反应器中加入浓盐酸浸取,因二氧化硅不反应,经过滤可得到废渣为二氧化硅,溶液a中含有Fe3+、Al3+、Cr3+等,加入碳酸钠溶液调节pH8.5~9.5,可除去Fe3+、Al3+,得到的废渣为Al(OH)3和Fe(OH)3,在CrO22-溶液中加入过氧化氢,经氧化可得到CrO42-溶液,然后加入Pb(NO3)2溶液,可得到PbCrO4沉淀,过滤后废液中含有Pb(NO3)2,加入明矾可得到硫酸铅,(1)将铬污泥粉碎可以增大与盐酸的接触面积,有利于提高浸取率;故答案为:增大接触面积,提高浸取率;(2)Ksp[Al(OH)3]=c(Al3+)?c3(OH-)=1.3*10-33,水解平衡常数Kh=c3(H+) c(Al3+) ,故Ksp[Al(OH)3]?Kh=(kw)3=(10-14)3=10-42,所以Kh=10?42 1.3*10?33 =7.7*10-10;故答案为:7.7*10-10;(3)由流程图可知,加入30%H2O2的目的是在碱性条件下将CrO2-氧化为CrO42-,同时生成水,反应离子方程式为3H2O2+2CrO2-+2OH-=2CrO42-+4H2O;故答案为:3H2O2+2CrO2-+2OH-=2CrO42-+4H2O;(4)检验沉淀是否完全的方法是:静置分层后,取上层清液,继续滴加Pb(NO3)2溶液,无沉淀生成,说明沉淀完全;故答案为:静置分层后,取上层清液,继续滴加Pb(NO3)2溶液,无沉淀生成,说明沉淀完全;(5)废液中含有Pb(NO3)2,废液中加入10%明矾溶液目的是将Pb2+转化为PbSO4沉淀,反应方程式为2Pb(NO3)2+KAl(SO4)2=2PbSO4↓+KNO3+Al(NO3)3;故答案为:2Pb(NO3)2+KAl(SO4)2=2PbSO4↓+KNO3+Al(NO3)3.
4, 铬酸铅(PbCrO4)俗称铬黄,不溶于水.广泛用于涂料、油墨、漆布、...
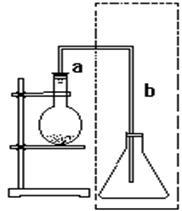
铬酸铅可以溶于硝酸,铬酸铅溶于碱液、无机酸,不溶于水,不溶于油类。铬酸铅又称铬黄,密度6.12g/cm3,熔点844℃。不溶于水、油和醋酸,溶于强碱和无机强酸。遇硫化氢变为黑色,遇碱变为橙红色。着色力和遮盖力强。不能与立德粉及群青共用。有毒。色光随原料配比和制备条件而异,有橘铬黄、深铬黄、中铬黄、浅铬黄、柠檬黄等五种。用作油性合成树脂涂料、印刷油墨、水彩和油彩的颜料,色纸、橡胶和塑料制品的着色剂。铬酸铅的危害:该物质可通过吸入其气溶胶及粉尘和经食入吸收到体内,急性中毒:吸入后对上呼吸道有刺激性;摄入后可引起头晕、头痛、恶心、呕吐、胃肠道刺激,可致死。慢性影响:可引起贫血、肾损害、铅蓄积、铅中毒。可引起皮炎和湿疹。铬化合物可引起铬鼻病和皮肤溃疡。国际癌症研究中心(IARC)将“铬和某些铬化合物”列入对人类致癌的化学物质。反复或长期与皮肤接触可能引起皮炎和慢性溃疡。可能引起皮肤过敏。参考资料来源:搜狗百科——铬酸铅
名词解释
NO3
硝酸根是指硝酸盐的阴离子,化学式:NO₃﹣,硝酸根为-1价,其中N为最高价+5价。
10
10,相当于汉字\"十\"。是位于9与11之间的自然数、正整数。 在十进制中,10是最小的两位数,写法是一个1后面加一个0,是一个合数,有4个因数(约数),是一个有理数。
溶液
溶液是由至少两种物质组成的均一、稳定的混合物,被分散的物质( 溶质)以分子或更小的质点分散于另一物质(溶剂)中。物质在 常温时有固体、液体和气体三种 状态。因此溶液也有三种状态,大气本身就是一种气体溶液, 固体溶液混合物常称固溶体,如合金。一般溶液只是专指液体溶液。液体溶液包括两种,即能够导电的 电解质溶液和不能导电的 非电解质溶液。所谓胶体溶液,更确切的说应称为 溶胶。其中,溶质相当于 分散质,溶剂相当于分散剂。在生活中常见的溶液有蔗糖溶液、碘酒、澄清石灰水、稀盐酸、盐水、空气等。